2023年辽宁葫芦岛中考化学试题及答案
可能用到的相对原子质量:H-1 C-12 O-16 Ca-40
第一部分选择题(共20分)
一、选择题(本题包括15个小题,共20分,每小题只有一个选项符合题意。第1小题~第10小题,每小题1分;第11小题~第15小题,每小题2分)
1. 劳动创造美好生活。下列班级劳动中涉及化学变化的是
A. 清扫灰尘 B. 擦拭黑板 C. 教室消毒 D. 花草浇水
2. 央视栏目《典籍里的中国》展现了中国智慧。用墨书写的典籍保存至今仍不变色,体现了碳单质具有的性质是
A. 质软 B. 导电性 C. 可燃性 D. 常温稳定性
3. “庄稼一枝花,全靠肥当家”。下列物质能用作钾肥的是
A. ![]() B. KCl C.
B. KCl C. ![]() D.
D. ![]()
4. 在“粗盐中难溶性杂质的去除”实验中,下列操作中正确的是
A. 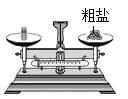 称量B.
称量B.  溶解 C.
溶解 C.  过滤 D.
过滤 D.  蒸发
蒸发
5. “中国天眼”FAST的“眼镜片”是由金刚砂(SiC)制造。金刚砂中碳元素的化合价为-4,则硅元素的化合价为
A. +1 B. +2 C. +3 D. +4
6. 在自来水生产过程中,没有用到的操作是
A. 沉淀 B. 过滤 C. 吸附 D. 蒸馏
7. 化学元素与人体健康紧密相关。为了预防甲状腺肿大应适当摄入的元素是
A. 铁 B. 锌 C. 碘 D. 钙
8. 守住良田沃土,保障粮食安全。某农田改良后土壤的pH为5.4,下表所列作物适宜在该农田种植的是
作物名称 | 马铃薯 | 油菜 | 水稻 | 萝卜 |
适宜生长的pH | 4.8~5.5 | 5.8~6.7 | 6.0~7.0 | 7.0~7.5 |
A. 马铃薯 B. 油菜 C. 水稻 D. 萝卜
9. 6月5日是世界环境日,今年我国的主题是“建设人与自然和谐共生的现代化”。下列做法符合该主题的是
A. 多使用一次性餐具 B. 废旧电池就地掩埋
C. 露天焚烧塑料垃圾 D. 养成节水节电习惯
10. 侯德榜发明的侯氏制碱法为我国化学工业作出了杰出的贡献。其主要反应为:![]()
![]() ,其中X的化学式是
,其中X的化学式是
A. NaCl B. ![]() C. NaClO D.
C. NaClO D. ![]()
11. 现有铝、铜、银三种金属,另选一种试剂就可验证它们的金属活动性强弱,该试剂是
A. 稀硫酸 B. 硝酸镁溶液 C. 硝酸铜溶液 D. 硝酸铝溶液
12. 下列物质属于单质的是
A. 钢 B. 银 C. 干冰 D. 冰水混合物
13. 化学学科与人类生活和社会发展关系密切。下列说法正确的是
A. 使用乙醇汽油可以节约石油资源
B. 霉变的食物煮熟后可放心食用
C. 防治水体污染是爱护水资源的唯一途径
D. 为了方便学习,可将实验室剩余药品带回家做实验
14. 化学学科核心素养展现了化学课程对学生发展的重要价值。下列说法错误的是
A. 化学观念:物质由微观粒子构成
B. 科学思维:有机化合物都含有碳元素,则含碳元素的化合物都是有机化合物
C. 科学探究与实践:将1~2小粒碘分别加入5mL水和5mL汽油中,可探究影响物质溶解性的因素
D. 科学态度与责任:可燃性气体遇明火易发生爆炸,加油站要严禁明火
15. 区分下列各种物质的实验方法正确的是
选项 | 需区分的物质 | 实验方法 |
A | 硬水和软水 | 加入肥皂水,搅拌 |
B | 纯金和黄铜 | 观察颜色 |
C | 二氧化碳和氮气 | 伸入燃着的木条 |
D | 氢氧化钠溶液和碳酸钠溶液 | 滴加无色酚酞溶液 |
A. A B. B C. C D. D
第二部分非选择题(共60分)
二、填空题(本题包括4个小题,每空1分,共18分)
16. 化学在生产、生活中有着广泛应用。现有①![]() ②
②![]() ③CaO④
③CaO④![]() 四种物质,请用物质前的数字序号填空。
四种物质,请用物质前的数字序号填空。
(1)可作燃料的是_____;
(2)可作保护气的是_____;
(3)可作食品干燥剂的是_____;
(4)可用于治疗胃酸过多症的是_____。
17. 2023年5月30日,神舟十五号、十六号乘员组在太空胜利会师,一起见证中国航天高光时刻。请回答。
(1)空间站太阳能电池板![]() 将太阳能转化为_____能。
将太阳能转化为_____能。
(2)舱外宇航服中,向航天员输送的可供给呼吸的气体是_____。最外层使用一种叫“特氟隆”的合成纤维,属于_____(填“金属材料”或“合成材料”)。
(3)返回舱返回时动力来自液氢和液氧,在即将着陆前要迅速释放剩余燃料,这样做的目的是_____。成功着陆后,航天员的营养餐包括鸡汤面、猪肉大葱水饺、煎鸡蛋及青菜等,其中含有的营养素有_____(填一种)。
18. 在新材料研发领域,我国科研人员做出杰出贡献。
(1)钼合金是核反应堆的高强韧材料,钼元素在元素周期表中信息如图1所示。

①钼属于_____(填“金属元素”或“非金属元素”)。
②钼的相对原子质量为_____。
(2)纳米催化剂应用于二氧化碳的转化,图2是其反应的微观示意图。
①反应中共有_____种氧化物。
②反应物的分子个数比为_____。
③反应中没有发生改变的是_____(填“分子”或“原子”)。
19. 如图1所示,![]() ℃时,将等质量的
℃时,将等质量的![]() 和KCl分别加入100g水中充分溶解后,升温至
和KCl分别加入100g水中充分溶解后,升温至![]() ℃。图2是
℃。图2是![]() 和KCl的溶解度曲线。
和KCl的溶解度曲线。

(1)图1烧杯甲中溶解的物质是_____。
(2)![]() ℃时,烧杯乙中的溶液是_____(填“饱和”或“不饱和”)溶液。
℃时,烧杯乙中的溶液是_____(填“饱和”或“不饱和”)溶液。
(3)若![]() 中混有少量KCl,可采用_____的方法提纯
中混有少量KCl,可采用_____的方法提纯![]() 。
。
(4)![]() ℃时,将50g
℃时,将50g![]() 固体放入50g水中充分溶解,所得溶液的溶质质量分数为_____。
固体放入50g水中充分溶解,所得溶液的溶质质量分数为_____。
三、简答题(本题包括3个小题,共16分)
20. 能源结构的改变,体现了社会的进步和发展。
(1)化石燃料都是_____(填“可再生”或“不可再生”)能源。将煤粉碎后燃烧,其目的是_____。化石燃料的大量使用对环境造成的影响有_____(答一点)。
(2)氢气是最理想的清洁燃料,但目前在生活和生产中并没有被广泛使用的原因是_____。
(3)请你预测未来燃料发展的主要方向是_____。
21. 早在春秋战国时期,我国就开始生产和使用铁器。
【认识铁及其来源】
(1)铁元素在自然界中以_____(填“单质”或“化合物”)形式存在。
(2)工业上从含有金属元素并有开采价值的矿石中提炼金属。赤铁矿是常见铁矿石,其主要成分的化学式为_____。
【认识铁的性质】
(3)菜刀、锤子用铁制而不用铝制,是利用铁具有_____的性质。
(4)将铁片放入硫酸锌和硫酸铜混合溶液中,写出发生反应的化学方程式_____。
【铁的锈蚀和防护】
(5)下列环境中的铁制品最容易生锈的是_____(填字母)。
A. 未擦干的铁锅 B. 喷油漆的栏杆 C. 盛水的不锈钢水杯
22. 同学们学习了酸、碱、盐等物质的相关知识后,构建了以碳酸钠为中心物质的网络关系图。其中甲、乙、丙、丁分别是初中常见的不同类别化合物,丁是常见的温室气体。各物质间的关系如下图所示(“――”表示相邻两种物质能发生反应;“→”表示两种物质间的转化关系;图中部分反应物、生成物及反应条件已略去)。请回答。
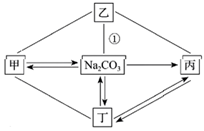
(1)甲的化学式为_____。
(2)若乙中只含两种元素,反应①的化学方程式为_____。
(3)若丙是大理石的主要成分,其用途是_____。
(4)甲和丁的反应_____(填“属于”或“不属于”)复分解反应。
四、实验题(本题包括3个小题,共18分)
23. 装置气密性良好是实验成功的基本保障。根据下图所示实验回答问题。
A.检查装置气密性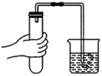 B.测空气中氧气含量
B.测空气中氧气含量
C.溶解时的吸、放热现象 D.验证质量守恒定律
D.验证质量守恒定律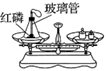
(1)实验A:观察到水中导管口有气泡冒出,请从分子的角度解释出现此现象的原因_____。
(2)实验B:若装置漏气,会使测得的实验结果_____(填“偏大”或“偏小”)。
(3)实验C:加入硝酸铵后,液面a处变化情况为_____(填“上升”或“下降”)。
(4)实验D:为确保实验成功,必须在_____容器中进行实验。
24. 化学是一门以实验为基础的科学。实验室制取氧气常用到下列装置,请回答。

(1)实验室用装置A制取氧气,其反应的化学方程式为_____。可以选择装置D收集氧气的原因是_____。
(2)实验室制气体时,选择装置B作为发生装置的依据是_____。
(3)实验时,装置B中长颈漏斗下端管口要伸入液面下的目的是_____。
(4)实验室检验氧气的方法是_____。
25. 在学习了酸、碱的性质后,为加深对酸和碱主要性质的认识,化学兴趣小组同学进行了如下实验活动。

(1)实验活动一:
在试管中加入约2mL硫酸铜溶液,然后滴入几滴氢氧化钠溶液,观察到有蓝色沉淀产生,溶液仍为蓝色。写出产生蓝色沉淀的化学方程式_____。继续向试管中加入稀硫酸,振荡,观察到蓝色沉淀消失。
【实验分析】
同学们对此时试管中溶液成分分析后认为:溶液中溶质一定有_____,可能有_____。
【实验验证】继续向试管中加入少量氢氧化钠溶液,振荡,观察到_____,证明了可能存在的物质是存在的。
(2)实验活动二:
同学们通过对比实验,验证了氢氧化钙的性质。
实验操作 | 实验现象 | 实验结论 |
向两支试管中各加入0.1g氢氧化钙粉末,分别加入10mL水和_____mL稀盐酸,振荡;再各滴入1~2滴酚酞溶液。 | _____ | 氢氧化钙溶液显碱性 |
试管甲中固体未完全溶解,试管乙中固体完全溶解,溶液为无色 | 氢氧化钙的性质为_____ |
通过以上实验,兴趣小组同学们对酸、碱的性质有了进一步的认识。
五、计算题(本题包括2个小题,共8分)
26. 荷叶中含有的荷叶碱(化学式为(C19H21NO2)具有降脂、抑菌等作用。请计算。
(1)一个荷叶碱分子中含有_____个原子。
(2)荷叶碱中碳、氢元素质量比为_____(填最简整数比)。
27. 好奇的同学们为了探测鸡蛋壳中碳酸钙的含量,从家里收集了鸡蛋壳清洗干燥后带到学校实验室。取11g鸡蛋壳样品于烧杯中,加入稀盐酸至不再产生气泡(假设鸡蛋壳中其他成分不与稀盐酸反应,生成气体全部逸出),共加入稀盐酸100g,此时烧杯内混合物的质量为106.6g。请计算。
(1)生成二氧化碳的质量为_____g。
(2)该鸡蛋壳中碳酸钙的质量分数。(结果保留到0.1%)
参考答案
第一部分选择题(共20分)
一、选择题(本题包括15个小题,共20分,每小题只有一个选项符合题意。第1小题~第10小题,每小题1分;第11小题~第15小题,每小题2分)
【1题答案】
【答案】C
【2题答案】
【答案】D
【3题答案】
【答案】B
【4题答案】
【答案】B
【5题答案】
【答案】D
【6题答案】
【答案】D
【7题答案】
【答案】C
【8题答案】
【答案】A
【9题答案】
【答案】D
【10题答案】
【答案】A
【11题答案】
【答案】C
【12题答案】
【答案】B
【13题答案】
【答案】A
【14题答案】
【答案】B
【15题答案】
【答案】A
第二部分非选择题(共60分)
二、填空题(本题包括4个小题,每空1分,共18分)
【16题答案】
【答案】(1)④ (2)①
(3)③ (4)②
【17题答案】
【答案】(1)电 (2) ①. 氧气##![]() ②. 合成材料
②. 合成材料
(3) ①. 防止发生爆炸(或减轻重量)(合理即可) ②. 蛋白质(合理即可)
【18题答案】
【答案】(1) ①. 金属元素 ②. 95.96
(2) ①. 两##2##二 ②. 2∶1##1∶2 ③. 原子
【19题答案】
【答案】(1)氯化钾##KCl
(2)不饱和
(3)降温结晶(或冷却热饱和溶液)
(4)50%
三、简答题(本题包括3个小题,共16分)
【20题答案】
【答案】(1) ①. 不可再生 ②. 增大可燃物与空气(或氧气)的接触面积,使之充分燃烧 ③. 酸雨(合理即可)
(2)氢气制取成本高(或贮存、运输困难)(合理即可)
(3)清洁化(或成本低、安全、便捷等)(合理即可)
【21题答案】
【答案】(1)化合物 (2)![]()
(3)硬度大 (4)![]() (5)A
(5)A
【22题答案】
【答案】(1)NaOH
(2)![]()
(3)建筑材料(或补钙剂)(合理即可)
(4)不属于
四、实验题(本题包括3个小题,共18分)
【23题答案】
【答案】(1)分子间有间隔,温度升高分子间隔变大
(2)偏小 (3)上升
(4)密闭
【24题答案】
【答案】(1) ①. ![]() (或
(或 ) ②. 氧气密度比空气大
) ②. 氧气密度比空气大
(2)反应物是固体和液体(或液体和液体),反应条件不需加热(合理即可)
(3)防止生成的气体从长颈漏斗中逸出
(4)将带火星木条伸入集气瓶中,若复燃则证明是氧气
【25题答案】
【答案】(1) ①. ![]() ②.
②. ![]() 、
、![]() ③.
③. ![]() ##硫酸 ④. 无蓝色沉淀产生(合理即可)
##硫酸 ④. 无蓝色沉淀产生(合理即可)
(2) ①. 10 ②. 试管甲中溶液由无色变为红色 ③. 微溶于水,能与盐酸反应
五、计算题(本题包括2个小题,共8分)
【26题答案】
【答案】(1)43 (2)76∶7
【27题答案】
【答案】(1)4.4 (2)解:设碳酸钙的质量为x。
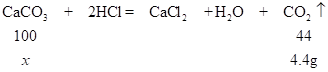
![]()
![]() g
g
碳酸钙的质量分数为:![]()
答:鸡蛋壳中碳酸钙的质量分数是90.9%。
