2025年河南普通高中学业水平选择性考试化学试题及答案
可能用到的相对原子质量:![]()
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求。
1. 活字印刷术极大地促进了世界文化![]() 交流,推动了人类文明的进步。下列“活字”字坯的主要成分为硅酸盐的是
交流,推动了人类文明的进步。下列“活字”字坯的主要成分为硅酸盐的是
| | | |
A.泥活字 | B.木活字 | C.铜活字 | D.铅活字 |
A. AB. BC. CD. D
2. 下列化学用语或图示正确的是
A. 反![]() 二氟乙烯的结构式:
二氟乙烯的结构式: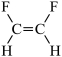
B. 二氯甲烷分子的球棍模型: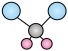
C. 基态S原子的价电子轨道表示式:![]()
D. 用电子式表示![]() 的形成过程:
的形成过程:![]()
3. 下列图示中,实验操作或方法符合规范的是
| | | |
A.溶解氯化钠固体 | B.量取 | C.收集二氧化碳气体 | D.观察钠与水的反应 |
A. AB. BC. CD. D
4. X是自然界中一种常见矿物的主要成分,可以通过如图所示的四步反应转化为Q(略去部分参与反应的物质和反应条件)。已知X和Q的组成元素相同。

下列说法错误的是
A. Y常用作油漆、涂料等的红色颜料B. 溶液Z加热煮沸后颜色会发生变化
C. ![]() 反应需要在强酸性条件下进行D. Q可以通过单质间化合反应制备
反应需要在强酸性条件下进行D. Q可以通过单质间化合反应制备
5. 对于下列过程中发生的化学反应。相应离子方程式正确的是
A. 磷酸二氢钠水解:![]()
B. 用稀盐酸浸泡氧化银:![]()
C. 向次氯酸钠溶液中加入碘化氢溶液:![]()
D. 向硫酸氢钠溶液中滴加少量碳酸氢钡溶液:![]()
6. 我国科研人员合成了一种深紫外双折射晶体材料,其由原子序数依次增大![]() 五种短周期元素
五种短周期元素![]() 和Z组成。基态X原子的s轨道中电子总数比p轨道中电子数多
和Z组成。基态X原子的s轨道中电子总数比p轨道中电子数多![]() 所在族的族序数等于Q的质子数,基态Y和Z原子的原子核外均只有1个未成对电子,且二者核电荷数之和为Q的4倍。下列说法正确的是
所在族的族序数等于Q的质子数,基态Y和Z原子的原子核外均只有1个未成对电子,且二者核电荷数之和为Q的4倍。下列说法正确的是
A. ![]() 为极性分子B.
为极性分子B. ![]() 为共价晶体
为共价晶体
C![]() 原子半径:
原子半径:![]() D. 1个
D. 1个![]() 分子中有2个
分子中有2个![]() 键
键
7. 化合物M是从红树林真菌代谢物中分离得到的一种天然产物,其结构如图所示。下列有关M的说法正确的是

A. 分子中所有的原子可能共平面
B. ![]() 最多能消耗
最多能消耗![]()
C. 既能发生取代反应,又能发生加成反应
D. 能形成分子间氢键,但不能形成分子内氢键
8. 某同学设计以下实验,探究简单配合物的形成和转化。

下列说法错误![]() 是
是
A. ②中沉淀与④中沉淀不是同一种物质
B. ③中现象说明配体与![]() 的结合能力:
的结合能力:![]()
C. ④中深蓝色物质在乙醇中的溶解度比在水中小
D. 若向⑤中加入稀硫酸,同样可以得到黄绿色溶液
9. 自旋交叉化合物在分子开关、信息存储等方面具有潜在的应用价值。某自旋交叉化合物的结构及在氯气气氛下的热重曲线分别如图1和图2所示。该化合物的相对分子质量![]() (x为整数)。
(x为整数)。
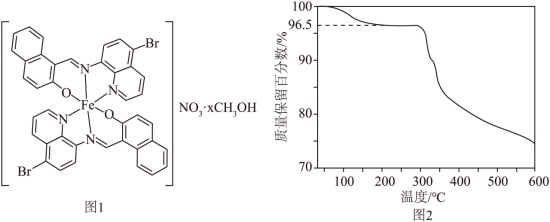
下列说法正确的是
A. ![]() B. 第一电离能:
B. 第一电离能:![]()
C. 该化合物中不存在离子键D. 该化合物中配位数与配体个数相等
10. 在催化剂a或催化剂b作用下,丙烷发生脱氢反应制备丙烯,总反应的化学方程式为![]() ,反应进程中的相对能量变化如图所示(*表示吸附态,
,反应进程中的相对能量变化如图所示(*表示吸附态,![]() 中部分进程已省略)。
中部分进程已省略)。
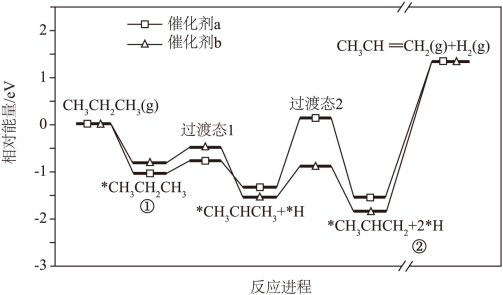
下列说法正确的是
A. 总反应是放热反应
B. 两种不同催化剂作用下总反应的化学平衡常数不同
C. 和催化剂b相比,丙烷被催化剂a吸附得到的吸附态更稳定
D. ①转化为②的进程中,决速步骤为![]()
11. 可持续高分子材料在纺织、生物医用等领域具有广阔的应用前景。一种在温和条件下制备高性能可持续聚酯P的路线如图所示。
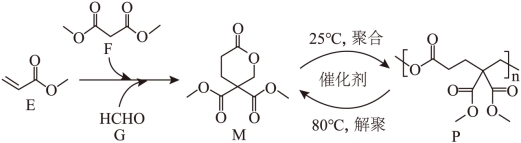
下列说法错误的是
A. E能使溴的四氯化碳溶液褪色
B. 由![]() 和G合成M时,有
和G合成M时,有![]() 生成
生成
C. P在碱性条件下能够发生水解反应而降解
D. P解聚生成M的过程中,存在![]() 键的断裂与形成
键的断裂与形成
12. 一种液流电解池在工作时可以实现海水淡化,并以![]() 形式回收含锂废弃物中的锂元素,其工作原理如图所示。
形式回收含锂废弃物中的锂元素,其工作原理如图所示。
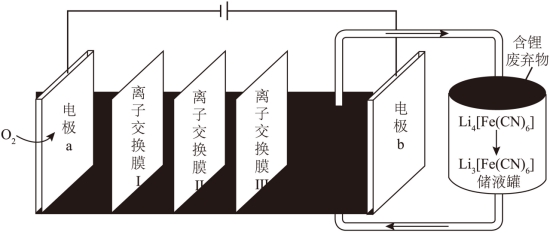
下列说法正确的是
A. Ⅱ为阳离子交换膜
B. 电极a附近溶液的![]() 减小
减小
C. 电极b上发生的电极反应式为![]()
D. 若海水用![]() 溶液模拟,则每脱除
溶液模拟,则每脱除![]() ,理论上可回收
,理论上可回收![]()
13. 在![]() 负载的
负载的![]() 催化剂作用下,
催化剂作用下,![]() 可在室温下高效转化为
可在室温下高效转化为![]() ,其可能的反应机理如图所示。
,其可能的反应机理如图所示。
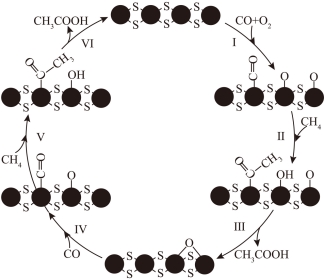
下列说法错误的是
A. 该反应的原子利用率为![]()
B. 每消耗![]() 可生成
可生成![]()
C. 反应过程中,![]() 和
和![]() 的化合价均发生变化
的化合价均发生变化
D. 若以![]() 为原料,用
为原料,用![]() 吸收产物可得到
吸收产物可得到![]()
14. 乙二胺(![]() ,简写为Y)可结合
,简写为Y)可结合![]() 转化为
转化为![]() (简写为
(简写为![]() )
)![]() (简写为
(简写为![]() )。
)。![]() 与Y可形成
与Y可形成![]() 和
和![]() 两种配离子。室温下向
两种配离子。室温下向![]() 溶液中加入Y,通过调节混合溶液的
溶液中加入Y,通过调节混合溶液的![]() 改变Y的浓度,从而调控不同配离子的浓度(忽略体积变化)。混合溶液中
改变Y的浓度,从而调控不同配离子的浓度(忽略体积变化)。混合溶液中![]() 和Y的初始浓度分别为
和Y的初始浓度分别为![]() 和
和![]() 。
。![]() 与
与![]() 的变化关系如图1所示(其中M代表
的变化关系如图1所示(其中M代表![]() 、
、![]() 或
或![]() ),分布系数
),分布系数![]() 与
与![]() 的变化关系如图2所示(其中N代表Y、
的变化关系如图2所示(其中N代表Y、![]() 或
或![]() )。比如
)。比如 。
。
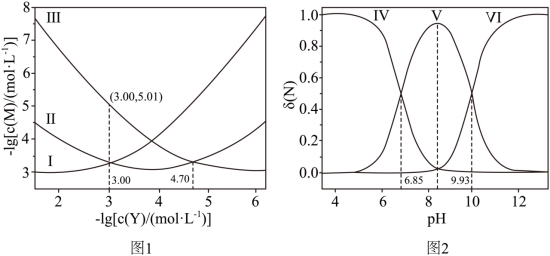
下列说法错误的是
A. 曲线I对应的离子是![]()
B. ![]() 最大时对应的
最大时对应的![]()
C. 反应![]() 的平衡常数
的平衡常数![]()
D. ![]() 时,
时,![]()
二、非选择题:本题共4小题,共58分。
15. 一种从预处理得到的贵金属合金粉[主要成分为![]() 、
、![]() (铑)、
(铑)、![]() ,含有少量
,含有少量![]() ]中尽可能回收铑的工艺流程如下:
]中尽可能回收铑的工艺流程如下:
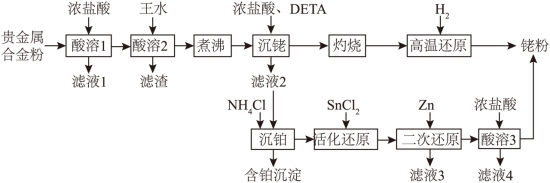
回答下列问题:
(1)“酸溶1”的目的是_______。
(2)已知“酸溶2”中![]() 转化为
转化为![]() ,则生成该物质的化学方程式为_______;“滤渣”的主要成分是_______(填化学式)。
,则生成该物质的化学方程式为_______;“滤渣”的主要成分是_______(填化学式)。
(3)“沉铑”中得到的沉淀经“灼烧”后分解成铑单质,但夹杂少量![]() 和
和![]() ,则“高温还原”中发生反应的化学方程式为_______。
,则“高温还原”中发生反应的化学方程式为_______。
(4)若“活化还原”在室温下进行,![]() 初始浓度为
初始浓度为![]() ,为避免生成
,为避免生成![]() 沉淀,溶液适宜的
沉淀,溶液适宜的![]() 为_______(填标号)[已知
为_______(填标号)[已知![]() 的
的![]() ]。
]。
A.2.0 B.4.0 C.6.0
(5)“活化还原”中,![]() 必须过量,其与
必须过量,其与![]() (III)反应可生成
(III)反应可生成![]() ,提升了
,提升了![]()
![]() 还原速率,该配离子中
还原速率,该配离子中![]() 的化合价为_______;反应中同时生成
的化合价为_______;反应中同时生成![]() ,
,![]() (III)以
(III)以![]() 计,则理论上
计,则理论上![]() 和
和![]() (III)反应的物质的量之比为_______。
(III)反应的物质的量之比为_______。
(6)“酸溶3”的目的是_______。
16. 某研究小组设计了如下实验测定某药用硫黄中硫的含量,其中硫转化的总反应为![]() 。
。
主要实验步骤如下:
Ⅰ.如图所示,准确称取![]() 细粉状药用硫黄于①中,并准确加入
细粉状药用硫黄于①中,并准确加入![]() 乙醇溶液(过量),加入适量蒸馏水,搅拌,加热回流。待样品完全溶解后,蒸馏除去乙醇。
乙醇溶液(过量),加入适量蒸馏水,搅拌,加热回流。待样品完全溶解后,蒸馏除去乙醇。
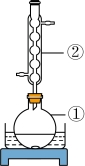
Ⅱ.室温下向①中加入适量蒸馏水,搅拌下缓慢滴加足量![]() 溶液,加热至
溶液,加热至![]() ,保持
,保持![]() ,冷却至室温。
,冷却至室温。
Ⅲ.将①中溶液全部转移至锥形瓶中,加入2滴甲基橙指示剂,用![]() 标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗![]() 溶液体积为
溶液体积为![]() 。
。
Ⅳ.不加入硫黄,重复步骤Ⅰ、Ⅱ、Ⅲ做空白实验,消耗![]() 标准溶液体积为
标准溶液体积为![]() 。计算样品中硫的质量分数。
。计算样品中硫的质量分数。
Ⅴ.平行测定三次,计算硫含量的平均值。
回答下列问题:
(1)仪器①的名称是:_______;②的名称是_______。
(2)步骤Ⅰ中,乙醇的作用是_______。
(3)步骤Ⅰ中,样品完全溶解后,必须蒸馏除去乙醇的原因是_______。
(4)步骤Ⅱ中不宜采用水浴加热的原因是_______。步骤Ⅱ结束后,若要检验反应后溶液中的![]() ,实验操作是_______。
,实验操作是_______。
(5)步Ⅲ中,判断滴定达到终点的现象为_______。
(6)单次样品测定中硫的质量分数可表示为_______(写出计算式)。
17. ![]() 的热分解与
的热分解与![]() 催化的
催化的![]() 重整结合,可生产高纯度合成气
重整结合,可生产高纯度合成气![]() ,实现碳资源的二次利用。主要反应如下:
,实现碳资源的二次利用。主要反应如下:
反应Ⅰ:![]()
反应Ⅱ:![]()
反应Ⅲ:![]()
回答下列问题:
(1)![]() 位于元素周期表中_______区;基态
位于元素周期表中_______区;基态![]() 的价电子排布式为_______。
的价电子排布式为_______。
(2)水分子的![]() 模型与其空间结构模型不同,原因是_______。
模型与其空间结构模型不同,原因是_______。
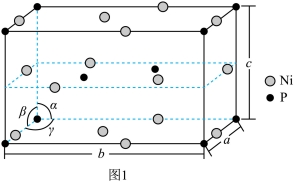
(3)![]() 的晶胞如图1所示(晶胞参数
的晶胞如图1所示(晶胞参数![]() ),该物质的化学式为_______。
),该物质的化学式为_______。
(4)恒压条件下,![]() 重整反应可以促进
重整反应可以促进![]() 分解,原因是_______。
分解,原因是_______。
(5)在温度分别为![]() 和
和![]() 下,
下,![]() 的平衡转化率与压强的关系如图2所示,反应温度最高的是_______(填“
的平衡转化率与压强的关系如图2所示,反应温度最高的是_______(填“![]() ”“
”“![]() ”或“
”或“![]() ”),原因是_______。
”),原因是_______。

(6)一定温度、![]() 下,向体系中加入
下,向体系中加入![]() 和
和![]() ,假设此条件下其他副反应可忽略,恒压反应至平衡时,体系中
,假设此条件下其他副反应可忽略,恒压反应至平衡时,体系中![]() 转化率为
转化率为![]() ,
,![]() 转化率为
转化率为![]() ,
,![]() 物质的量为
物质的量为![]() ,反应Ⅲ的平衡常数
,反应Ⅲ的平衡常数![]() _______(保留小数点后一位),此时原位
_______(保留小数点后一位),此时原位![]() 利用率为_______。
利用率为_______。
已知:原位![]() 利用率
利用率
18. 化合物I具有杀虫和杀真菌活性,以下为其合成路线之一(部分反应条件已简化)。
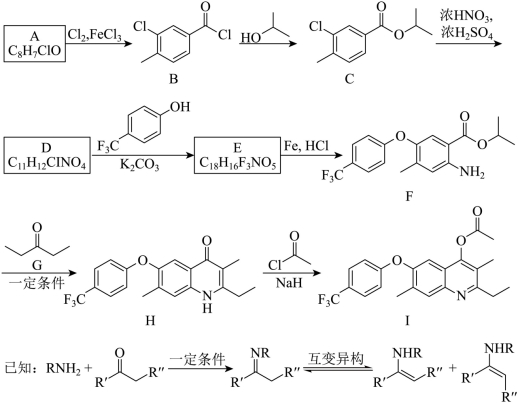
回答下列问题:
(1)I中含氧官能团的名称是_______。
(2)A的结构简式为_______。
(3)由B生成C的化学方程式为_______。反应时,在加热搅拌下向液体B中滴加异丙醇;若改为向异丙醇中滴加B则会导致更多副产物的生成,副产物可能的结构简式为_______(写出一种即可)。
(4)由D生成E的反应类型为_______。
(5)由F生成H的反应中可能生成中间体J,已知J的分子式为![]() ,则J的结构简式为_______(写出一种即可)。
,则J的结构简式为_______(写出一种即可)。
(6)G的同分异构体中,含有碳氧双键的还有_______种(不考虑立体异构);其中,能发生银镜反应,且核磁共振氢谱显示为两组峰的同分异构体的结构简式为_______。
参考答案
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求。
【1题答案】
【答案】A
【2题答案】
【答案】B
【3题答案】
【答案】B
【4题答案】
【答案】C
【5题答案】
【答案】A
【6题答案】
【答案】D
【7题答案】
【答案】C
【8题答案】
【答案】D
【9题答案】
【答案】A
【10题答案】
【答案】C
【11题答案】
【答案】B
【12题答案】
【答案】D
【13题答案】
【答案】B
【14题答案】
【答案】D
二、非选择题:本题共4小题,共58分。
【15题答案】
【答案】(1)溶解Fe,使其进入溶液,从而通过过滤实现分离
(2) ①. ![]() ②. SiO2
②. SiO2
(3)![]() 、
、![]()
(4)A (5) ①. +1 ②. 6:1
(6)除去滤渣中未反应的Zn
【16题答案】
【答案】(1) ①. 圆底烧瓶 ②. 球形冷凝管
(2)作溶剂,溶解单质硫
(3)防止双氧水氧化乙醇,影响实验测定结果
(4) ①. 实验需要加热至100 ℃ ②. 取适量混合液先加入盐酸酸化,无明显实验现象,再加入氯化钡溶液产生白色沉淀,说明含有![]()
(5)滴入最后半滴盐酸,溶液颜色由黄色变为橙色,且半分钟内不褪色
(6)![]()
【17题答案】
【答案】(1) ①. s ②. 3d8
(2)O原子上存在2对孤电子对
(3)Ni2P (4)反应Ⅱ消耗反应Ⅰ产生的CO2,降低体系CO2分压,使反应Ⅰ平衡右移
(5) ①. T1 ②. 升高温度,反应Ⅱ正向移动
(6) ①. 1.2 ②. 70%
【18题答案】
【答案】(1)醚键,酯基
(2)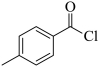 (3) ①.
(3) ①. 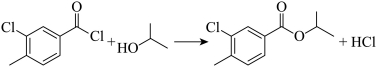 ②.
②. 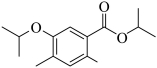
(4)取代反应 (5)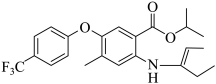
(6) ①. 6 ②.