2024�갲�ո߿���ѧ���⼰��
���������õ������ԭ��������![]()
����һ��ѡ���⣺���14С�⣬ÿС��3�֣���42�֡���ÿС��������ĸ�ѡ���У�ֻ��һ���Ƿ�����ĿҪ��ġ�
����1. ������Դ�����У��ڸ�������������ת����ϵ��ȷ����
����A. ú![]() ú�� B. ʯ��
ú�� B. ʯ��![]() ��ϩ C. ��֬
��ϩ C. ��֬![]() ���� D. ����
���� D. ����![]() �Ҵ�
�Ҵ�
����2. ���и������ʵļ����У������е���
����A. �������ƺ���ƣ���ˮ���� B. ˮ���Ͳ�����X��������ʵ��
����C. �Ȼ��ƺ��Ȼ��أ���ɫ���� D. ���ͼױ����μ���ˮ����
����3. ���������ȿ������Ͷ�ϰ�ߣ�Ҳ�ܽ���ѧ֪ʶӦ����ʵ���������йؽ��ͺ�������
����A. ��ϴ������ʱ���ɣ��ܼ�����������������ʴ������
����B. ����ʳ��ĺ��ڼ���ʳ�Σ��ܱ���![]() ��ʱ�����ȶ��ֽ�
��ʱ�����ȶ��ֽ�
����C. �����ǰ��Ƴɽ���֭���������Ǹ����³��̿��Ϊʳ����ɫ
����D. �������ʱ����ʳ�ô������![]() �кͷ����̲�������
�кͷ����̲�������
����4. ����ѡ���е������ܰ�ͼʾ·������Ȼ����ת�����Ҽ�ˮ����ֱ�������ҵ���
����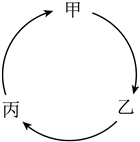
���� ѡ�� | ���� �� | ���� �� | ���� �� |
���� A | ���� | ���� | ���� |
���� B | ���� | ���� | ���� |
���� C | ���� | ���� | ���� |
���� D | ���� | ���� | ���� |
����A. A B. B C. C D. D
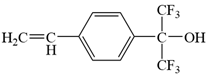
����5. D-��������������(�ṹ��ʽ����)��һ����Ȼ���ڵ����ⵥ�ǡ������йظ�����˵����ȷ����
����
����A. ����ʽΪ![]() B. �ܷ������۷�Ӧ
B. �ܷ������۷�Ӧ
����C. �������ǻ�Ϊͬϵ�� D. �����к���![]() ��������
��������![]() ��
��
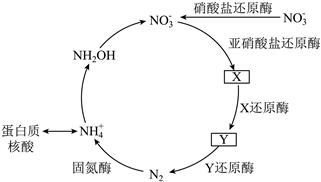
����6. �����ϵ����ﵪѭ���漰���ֺ������ʣ�ת����ϵ֮һ����ͼ��ʾ(X��Y��Ϊ��������)���ǰ�(![]() )���м�������ʽ����ѭ�������³�ѹ�£��ǰ��׳��⣬ˮ��Һ�ʼ��ԣ������ᷴӦ�IJ��������ǰ�
)���м�������ʽ����ѭ�������³�ѹ�£��ǰ��׳��⣬ˮ��Һ�ʼ��ԣ������ᷴӦ�IJ��������ǰ�![]() �㷺����ҩƷ�����ϵȵĺϳɡ�
�㷺����ҩƷ�����ϵȵĺϳɡ�
������֪![]() ʱ��
ʱ��![]() ��
��![]() ��
��![]() ��
��
����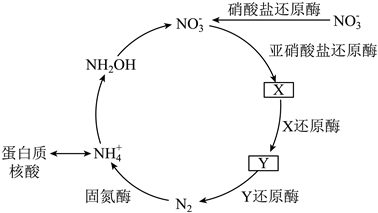
����NA�ǰ����ӵ�������ֵ������˵����ȷ����
����A. ��״���£�![]() ��Y�����������ԭ����Ϊ
��Y�����������ԭ����Ϊ![]()
����B. ![]() ��Һ��
��Һ��![]() ��
��![]() ����Ϊ
����Ϊ![]()
����C. ![]() ��ȫת��Ϊ
��ȫת��Ϊ![]() ʱ��ת�Ƶĵ�����Ϊ
ʱ��ת�Ƶĵ�����Ϊ![]()
����D. ![]() �к��еļ۵�������Ϊ
�к��еļ۵�������Ϊ![]()
����7. �����ϵ����ﵪѭ���漰���ֺ������ʣ�ת����ϵ֮һ����ͼ��ʾ(X��Y��Ϊ��������)���ǰ�(![]() )���м�������ʽ����ѭ�������³�ѹ�£��ǰ��׳��⣬ˮ��Һ�ʼ��ԣ������ᷴӦ�IJ��������ǰ�
)���м�������ʽ����ѭ�������³�ѹ�£��ǰ��׳��⣬ˮ��Һ�ʼ��ԣ������ᷴӦ�IJ��������ǰ�![]() �㷺����ҩƷ�����ϵȵĺϳɡ�
�㷺����ҩƷ�����ϵȵĺϳɡ�
������֪![]() ʱ��
ʱ��![]() ��
��![]() ��
��![]() ��
��
����
���������й����ʽṹ�����ʵıȽ��У���ȷ����
����A. ���ǣ�![]()
����B. �۵㣺![]()
����C. ![]() ͬŨ��ˮ��Һ��
ͬŨ��ˮ��Һ��![]()
����D. �ǰ����Ӽ������ǿ����![]()
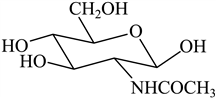
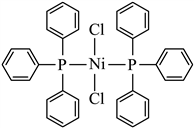
����8. ij�����ṹ��ʽ��ͼ��ʾ������˵���������
����
����A. ��������![]() Ϊ
Ϊ![]() �� B. ��̬ԭ�ӵĵ�һ�����ܣ�
�� B. ��̬ԭ�ӵĵ�һ�����ܣ�![]()
����C. ��������C��P����ȡ![]() �ӻ� D. ��̬
�ӻ� D. ��̬![]() ԭ�Ӽ۵����Ų�ʽΪ
ԭ�Ӽ۵����Ų�ʽΪ![]()
����9. �����±��ṩ���Լ�����Ʒ������ʵ����Ӧʵ��Ŀ�ĵ���
���� ѡ�� | ���� ʵ��Ŀ�� | ���� �Լ� | ���� ��Ʒ |
���� A | ���� �Ƚ�þ�����Ľ�����ǿ�� | ���� | ���� �Թܡ���ͷ�ι� |
���� B | ���� �Ʊ��������� | ���� �Ҵ������ᡢŨ���ᡢ���� | ���� �Թܡ����������ܡ��齺������̨(������)�����Ƭ���ƾ��ơ���� |
���� C | ���� �Ʊ� | ���� | ���� �Թܡ���ͷ�ι� |
���� D | ���� ��������ˮ���Ʊ� | ���� ���� | ���� �ձ�����ͷ�ιܡ�ʯ���������żܡ��ƾ��ơ���� |
����A. A B. B C. C D. D
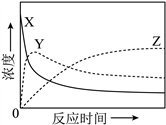
����10. ij�¶��£����ܱ������г���һ������![]() ���������з�Ӧ��
���������з�Ӧ��![]() ��
��![]() ����ø�����Ũ���뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ�����з�Ӧ����ʾ��ͼ�����������
����ø�����Ũ���뷴Ӧʱ��Ĺ�ϵ��ͼ��ʾ�����з�Ӧ����ʾ��ͼ�����������
����
����A. 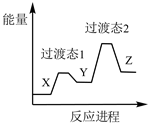 B.
B.  C.
C. 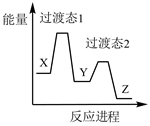 D.
D. 
����11. �ҹ�ѧ���з���һ������ˮϵп��أ���ʾ��ͼ���¡��õ�طֱ���![]() (�ֲ��ṹ���ע������ʾ)�γɵ��ȶ������Ӳ��Ϻ�
(�ֲ��ṹ���ע������ʾ)�γɵ��ȶ������Ӳ��Ϻ�![]() Ϊ�缫����
Ϊ�缫����![]() ��
��![]() ���ҺΪ�������Һ������˵���������
���ҺΪ�������Һ������˵���������
����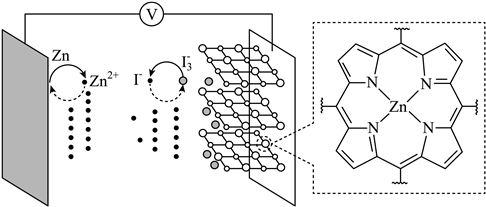
����A. ��ע������ʾ�ṹ�д��ڹ��ۼ�����λ��
����B. ����ܷ�ӦΪ��![]()
����C. ���ʱ����������ԭ��![]() ��Ҫ����
��Ҫ����![]()
����D. �ŵ�ʱ������![]() ��������ת��
��������ת��![]() ����
����
����12. �����£�Ϊ̽��������ȥ��ˮ����![]() ��Ӱ�����أ���ò�ͬ������
��Ӱ�����أ���ò�ͬ������![]() Ũ����ʱ��仯��ϵ����ͼ��
Ũ����ʱ��仯��ϵ����ͼ��
����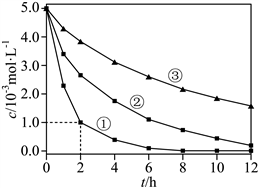
���� ʵ����� | ���� ˮ�����/ | ���� ����������/ | ���� ˮ����ʼ |
���� �� | ���� 50 | ���� 8 | ���� 6 |
���� �� | ���� 50 | ���� 2 | ���� 6 |
���� �� | ���� 50 | ���� 2 | ���� 8 |
��������˵����ȷ����
����A. ʵ����У�0~2Сʱ��ƽ����Ӧ����![]()
����B. ʵ����У���Ӧ�����ӷ���ʽΪ��![]()
����C. ����������ͬʱ���ʵ����������������ɼӿ췴Ӧ����
����D. ����������ͬʱ��ˮ����ʼ![]() ԽС��
ԽС��![]() ��ȥ��Ч��Խ��
��ȥ��Ч��Խ��
����13. ������������ʦ�о�����![]() ��
��![]() ��
��![]() ����ˮ���е�
����ˮ���е�![]() ����֪
����֪![]() ʱ��
ʱ��![]() ������ҺŨ��ԼΪ
������ҺŨ��ԼΪ![]() ��
��![]() ��
��![]() ��
��![]() ��
��![]() ������˵���������
������˵���������
����A. ![]() ��Һ�У�
��Һ�У�![]()
����B. ![]() ��Һ�У�
��Һ�У�![]()
����C. ��![]() ����Һ�м���
����Һ�м���![]() ����ʹ
����ʹ![]()
����D. ��![]() ����Һ��ͨ��
����Һ��ͨ��![]() ���������ͣ�������Һ�У�
���������ͣ�������Һ�У�![]()
����14. �о���Ա�Ʊ���һ�־��������ͨ���ĵ���������(![]() )�������������͵���ʱ
)�������������͵���ʱ![]() Ǩ�ƹ�������ͼ��ʾ����֪����������
Ǩ�ƹ�������ͼ��ʾ����֪����������![]() Ϊ
Ϊ![]() �ۣ�
�ۣ�![]() Ϊ
Ϊ![]() �ۡ�����˵���������
�ۡ�����˵���������
����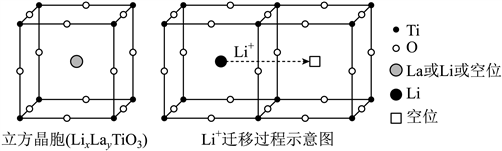
����A. ����ʱ��![]() ��
��![]() �ļ�̬���� B. ��
�ļ�̬���� B. ��![]() ��
��![]() ���λ����Ŀ���
���λ����Ŀ���
����C. ���������ڽ���Oԭ����Ϊ12 D. ����ʱ����λ�ƶ���������������෴
����������ѡ���⣺���4С�⣬��58�֡�
����15. ����ͭ������ͭ�������![]() �ȶ���Ԫ�ء��о���Ա�����һ�ִ�ͭ�������з������ս���������̣�����ͼ��ʾ��
�ȶ���Ԫ�ء��о���Ա�����һ�ִ�ͭ�������з������ս���������̣�����ͼ��ʾ��
����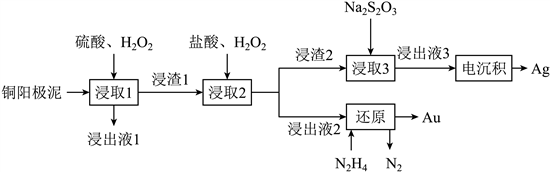
�����ش��������⣺
������1��![]() λ��Ԫ�����ڱ���_______���ڵ�_______�塣
λ��Ԫ�����ڱ���_______���ڵ�_______�塣
������2��������Һ1���к��еĽ���������Ҫ��_______��
������3������ȡ2�������У����ʽ�ת��Ϊ![]() �Ļ�ѧ����ʽΪ_______��
�Ļ�ѧ����ʽΪ_______��
������4������ȡ3�������У�������2���е�_______(�ѧʽ)ת��Ϊ![]() ��
��
������5����������������������ĵ缫��ӦʽΪ_______�����������������ɺ���������Һ�п�ѭ�����õ�����Ϊ_______(�ѧʽ)��
������6������ԭ�������У���������![]() �����
�����![]() �����ʵ���֮��Ϊ_______��
�����ʵ���֮��Ϊ_______��
������7��![]() �ɱ�
�ɱ�![]() ����Ϊ
����Ϊ![]() �������ʽṹ�ĽǶȷ���
�������ʽṹ�ĽǶȷ���![]() �ĽṹΪ(a)������(b)��ԭ��_______��
�ĽṹΪ(a)������(b)��ԭ��_______��
����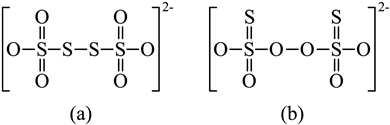
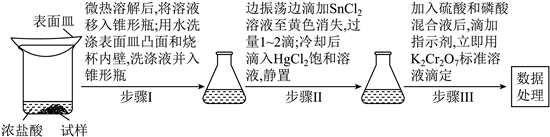
����16. �ⶨ����ʯ���������Ĵ�ͳ������![]() ���ζ������о�С���ø÷����ⶨ����Ϊ
���ζ������о�С���ø÷����ⶨ����Ϊ![]() ��ij�����������е���������
��ij�������������������
������������Һ��
������![]() ����Һ��
����Һ��
������![]() ��Һ����ȡ
��Һ����ȡ![]() ����
����![]() Ũ���ᣬ��ˮ��
Ũ���ᣬ��ˮ��![]() ����������������
����������������
�������ⶨ����������ͼ��ʾ(����װ��·ȥ)�����������ʵ�顣
����
������֪���Ȼ�������������������ʱ![]() ���ɽ�
���ɽ�![]() ����Ϊ
����Ϊ![]() ����������
����������![]() ��
��![]() �ɱ�
�ɱ�![]() ��ԭΪ
��ԭΪ![]() ���ش��������⣺
���ش��������⣺
������1�����������ڱ�ʵ���б����õ�����_______(������)��
����
������2��������ӷ���ʽ��������![]() ��Һʱ����������ԭ��_______��
��Һʱ����������ԭ��_______��
������3������I�С��ȡ���ԭ����_______��
������4����衢��У���δ�������ζ�������ᵼ�²ⶨ��������_______(�ƫ��ƫС�����䡱)��
������5��������![]() ����Һ
����Һ![]() ����
����![]() ������
������![]() ����������Ϊ_______(�ú�a��c��V�Ĵ���ʽ��ʾ)��
����������Ϊ_______(�ú�a��c��V�Ĵ���ʽ��ʾ)��
������6��![]() �ζ���Ҳ�ɲⶨ���ĺ���������Ҫԭ��������
�ζ���Ҳ�ɲⶨ���ĺ���������Ҫԭ��������![]() ��
��![]() ������ʯ������
������ʯ������![]() ��ԭΪ
��ԭΪ![]() ������
������![]() ����Һ�ζ���
����Һ�ζ���
�����ٴӻ����Ƕȷ������÷��������![]() ���ζ������ŵ���_______��
���ζ������ŵ���_______��
������Ϊ̽��![]() ��Һ�ζ�ʱ��
��Һ�ζ�ʱ��![]() �ڲ�ͬ����¶�
�ڲ�ͬ����¶�![]() �ⶨ�����Ӱ�죬�ֱ���������Һ�м���1��
�ⶨ�����Ӱ�죬�ֱ���������Һ�м���1��![]() ��Һ���������±���
��Һ���������±���
���� ��Һ | ���� ���� | |
���� �հ�ʵ�� | ���� | ���� �Ϻ�ɫ����ȥ |
���� ʵ��I | ���� | ���� �Ϻ�ɫ����ȥ |
���� ʵ�颢 | ���� | ���� �Ϻ�ɫ���Ա�dz |
���������Լ�XΪ_______�����ݸ�ʵ��ɵó��Ľ�����_______��
����17. ��ϩ��һ����;�㷺���л�����ԭ�ϡ�����������ϩ���о����ܹ�ע���ش��������⣺
��������������ϩ��
������1��![]() �������ⷴӦ��
�������ⷴӦ��
����![]()
![]()
����![]()
![]()
�������㣺![]()
![]() _______
_______![]()
������2��![]() ֱ�����ⷴӦΪ
ֱ�����ⷴӦΪ![]() ��
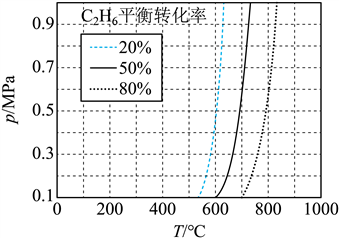
��![]() ��ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ��ͼ��ʾ����
��ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ��ͼ��ʾ����![]() _______0(�>����<����=��)�������ͼ�����������У��ﵽƽ��ʱת������ӽ�
_______0(�>����<����=��)�������ͼ�����������У��ﵽƽ��ʱת������ӽ�![]() ����_______(����)��
����_______(����)��
����
����a��![]() b��
b��![]() c��
c��![]()
������3��һ���¶Ⱥ�ѹǿ�¡���Ӧi ![]()
������Ӧ�� ![]() (
(![]() Զ����
Զ����![]() )(
)(![]() ����ƽ�����ʵ�����������ƽ��Ũ�ȼ����ƽ�ⳣ��)
����ƽ�����ʵ�����������ƽ��Ũ�ȼ����ƽ�ⳣ��)
�����ٽ�������Ӧiʱ��![]() ��ƽ��ת����Ϊ
��ƽ��ת����Ϊ![]() ������
������![]() _______��
_______��
������ͬʱ������Ӧi�͢�ʱ�����������Ӧi��ȣ�![]() ��ƽ�����_______(�������С�����䡱)��
��ƽ�����_______(�������С�����䡱)��
�������������ϩ������ķ��롿
������4��ͨ��![]() ���ε�Y����ɸ������-�Ѹ�����ʵ��
���ε�Y����ɸ������-�Ѹ�����ʵ��![]() ��
��![]() ������ķ��롣
������ķ��롣![]() ��_______��
��_______��![]() ���ӵ�
���ӵ�![]() �������γ���λ����������λ��ǿ�����ڷ��»������ۼ�֮�䡣�ø÷���ɸ����
�������γ���λ����������λ��ǿ�����ڷ��»������ۼ�֮�䡣�ø÷���ɸ����![]() ��
��![]() ���ŵ���_______��
���ŵ���_______��
������5�����³�ѹ�£���![]() ��
��![]() �������ϣ���һ������ͨ��ij����������������������Ũ��(c)�����Ũ��(
�������ϣ���һ������ͨ��ij����������������������Ũ��(c)�����Ũ��(![]() )֮����ʱ��仯��ϵ��ͼ��ʾ�������ƶϺ�������_______(����)��
)֮����ʱ��仯��ϵ��ͼ��ʾ�������ƶϺ�������_______(����)��
����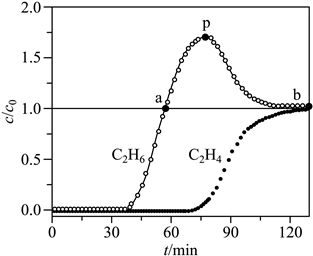
����A��ǰ![]() �����������δ������
����������������
����B��p���Ӧ��ʱ�̣������������Ҫ�ɷ���![]()
����C��a-b��Ӧ��ʱ����ڣ�������![]() ���±�
���±�![]() ���
���
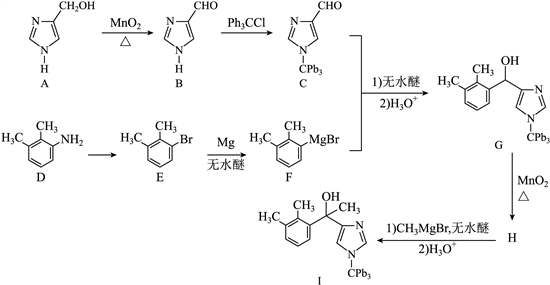
����18. ������1��һ��ҩ���м��壬��������·�ߺϳ�(![]() �������������ַ�Ӧ������ȥ)��
�������������ַ�Ӧ������ȥ)��
����
������֪��
����i) 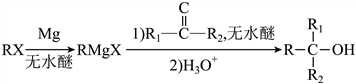
����ii)![]() ���뺬�����⻯����(
���뺬�����⻯����(![]() )��Ӧ��
)��Ӧ��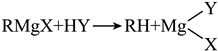
![]() ����
����![]() ��
��![]() ��
��![]() ��
��![]() �ȡ�
�ȡ�
������1��A��B�к������������Ʒֱ�Ϊ_______��_______��
������2��E��һ�������»�ԭ�õ�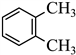 �����ߵĻ�ѧ����Ϊ_______��
�����ߵĻ�ѧ����Ϊ_______��
������3��H�Ľṹ��ʽΪ_______��
������4��E��F��Ӧ�С��������ʲ���������Ӧ�ܼ�����_______(����)��
����a��![]() b��
b��![]() c��
c�� ![]() d��
d��![]()
������5��D��ͬ���칹���У�ͬʱ����������������_______��(�����������칹)��д������һ��ͬ���칹��Ľṹ��ʽ_______��
�����ٺ�������̼ �ں���2��̼̼���� �۲�����
������6�����������ϳ�·�ߣ������![]() �Ͳ�����3��̼���л���Ϊԭ�ϣ��Ʊ�һ�ֹ�̽�����
�Ͳ�����3��̼���л���Ϊԭ�ϣ��Ʊ�һ�ֹ�̽�����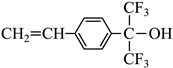 �ĺϳ�·��_______(�����Լ���ѡ)��
�ĺϳ�·��_______(�����Լ���ѡ)��
���
����һ��ѡ���⣺���14С�⣬ÿС��3�֣���42�֡���ÿС��������ĸ�ѡ���У�ֻ��һ���Ƿ�����ĿҪ��ġ�
����1�����𰸡�C
����2�����𰸡�D
����3�����𰸡�A
����4�����𰸡�D
����5�����𰸡�B
����6�����𰸡�A
����7�����𰸡�D
����8�����𰸡�C
����9�����𰸡�A ����10�����𰸡�B 11�����𰸡�C ���� ����13�����𰸡�B ����14�����𰸡�B ����������ѡ���⣺���4С�⣬��58�֡� ����15 �������𰸡���1�� ��. �� ��. ��B ������2��Cu2+ ��3�� ������4��AgCl ��5�� ��. ������6��3��4 ��7��(a)�ṹ�е����Ʒֲ��Ͼ��⣬�ṹ��Ϊ�ȶ���(b)�ṹ������������IJ��غϣ����Խϴϲ��ȶ����Ҵ��ڹ��������������������Դ���I2����Na2S2O3���ܱ�I2������(b)�ṹ ����16 �������𰸡� ������1������ƿ����Ͳ ������2��Sn2+�ױ���������ΪSn4+�����ӷ���ʽΪ ������3������ ������4��ƫС ��5�� ������6�� ��. ����ȫ���Ի������Ѻ� ��. H2O ��. ����Խǿ��KMnO4��������Խǿ��Cl-��KMnO4�����Ŀ�����Խ��Fe2+�ⶨ�����ɸ��ŵĿ�����Խ�������KMnO4��Һ���еζ�ʱ��Ҫ������Һ��pHֵ ����17 �������𰸡� ������1��-566 ������2�� ��. > ��. b ������3�� ��. ������4�� ��. 4s�չ�� ��. ʶ��ȸߣ�����Ч��C2H4��C2H6���룬������IJ����������٣����Ƚϸ� ������5��BC ����18 �������𰸡� ������1�� ��. �ǻ� ��. ȩ�� ������2��1��2-������(�ڶ��ױ�) ������3�� ������5�� ��. 4 ��. CH��C-CH2-CH2-CH2-CH(NH2)-C��CH ������6����![]()
![]() ��.
��. ![]()
![]() ������Sn��������Ӧ
������Sn��������Ӧ![]() ���ɷ�ֹSn2+����
���ɷ�ֹSn2+���� ![]() ���ܽ�ȣ��ٽ����ܽ�
���ܽ�ȣ��ٽ����ܽ� ![]()
![]() ��. ����
��. ���� 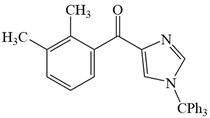 ��4��bc
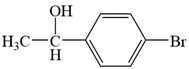
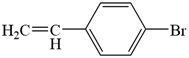
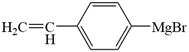
��4��bc 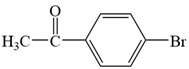
![]()
![]()
![]()
![]()