2024年5月上海普通高中学业水平等级性考试化学试题及答案
一、氟及其化合物
氟元素及其化合物具有广泛用途。
1. 下列关于氟元素的性质说法正确的是
A. 原子半径最小 B. 原子第一电离能最大
C. 元素的电负性最强 D. 最高正化合价为+7
2. 下列关于![]() 与
与![]() 说法正确的是
说法正确的是
A. 是同种核素 B. 是同素异形体
C. ![]() 比
比![]() 多一个电子 D.
多一个电子 D. ![]() 比
比![]() 多一个中子
多一个中子
3. 萤石(![]() )与浓硫酸共热可制备HF气体,写出该反应的化学方程式:_______,该反应中体现浓硫酸的性质是_______。
)与浓硫酸共热可制备HF气体,写出该反应的化学方程式:_______,该反应中体现浓硫酸的性质是_______。
A.强氧化性 B.难挥发性 C.吸水性 D.脱水性
4. 液态氟化氢(HF)的电离方式为:![]() ,其中X为_______。
,其中X为_______。![]() 的结构为
的结构为![]() ,其中
,其中![]() 与HF依靠_______相连接。
与HF依靠_______相连接。
5. 回答下列问题:
(1)氟单质常温下能腐蚀![]() 等金属,但工业上却可用
等金属,但工业上却可用![]() 制容器储存,其原因是_______。
制容器储存,其原因是_______。
![]() 是极强的氧化剂,用
是极强的氧化剂,用![]() 和
和![]() 可制备稀有气体离子化合物,六氟合铂氙
可制备稀有气体离子化合物,六氟合铂氙![]() 的制备方式如图所示
的制备方式如图所示
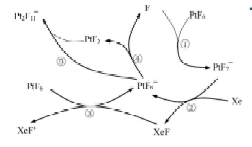
(2)上述反应中的催化剂为_______。
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
(3)上述过程中属于氧化还原反应的是_______。
A. ② B. ③ C. ④ D. ⑤
(4)氟气通入氙(Xe)会产生![]() 三种氟化物气体。现将
三种氟化物气体。现将![]() 的
的![]() 和
和![]() 的
的![]() 同时通入
同时通入![]() 的容器中,反应
的容器中,反应![]() 后,测得容器内共有
后,测得容器内共有![]() 气体,且三种氟化物的比例为
气体,且三种氟化物的比例为![]() ,则
,则![]() 内
内![]() 的速率
的速率![]() _______。
_______。
二、粗盐水的精制
6. 粗盐中含有![]() 等杂质离子,实验室按下面的流程进行精制:
等杂质离子,实验室按下面的流程进行精制:

已知:![]() 和
和![]() 的溶解度如图所示:
的溶解度如图所示:
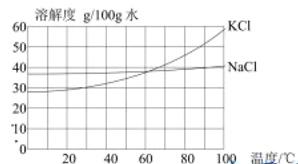
(1)步骤①中![]() 要稍过量。请描述检验
要稍过量。请描述检验![]() 是否过量的方法:_______。
是否过量的方法:_______。
(2)若加![]() 后不先过滤就加氢氧化钠和碳酸钠,会导致_______。
后不先过滤就加氢氧化钠和碳酸钠,会导致_______。
A. ![]() 不能完全去除 B. 消耗更多
不能完全去除 B. 消耗更多![]()
C. ![]() 不能完全去除 D. 消耗更多
不能完全去除 D. 消耗更多![]()
(3)过滤操作中需要的玻璃仪器。除烧杯和玻璃棒外,还需要_______。
A. 分液漏斗 B. 漏斗 C. 容量瓶 D. 蒸发皿
(4)步骤④中用盐酸调节pH至3~4,除去的离子有_______。
(5)“一系列操作”是指_______。
A. 蒸发至晶膜形成后,趁热过滤 B. 蒸发至晶膜形成后,冷却结晶
C. 蒸发至大量晶体析出后,趁热过滤 D. 蒸发至大量晶体析出后,冷却结晶
(6)请用离子方程式表示加入盐酸后发生的反应_______。
另有两种方案选行粗盐提纯。
方案2:向粗盐水中加入石灰乳[主要成分为![]() ]除去
]除去![]() ,再通入含
,再通入含![]() 的工业废气除去
的工业废气除去![]() ;
;
方案3:向粗盐水中加入石灰乳除去![]() ,再加入碳酸钠溶液除去
,再加入碳酸钠溶液除去![]() 。
。
(7)相比于方案3,方案2的优点是_______。
(8)已知粗盐水中![]() 含量为
含量为![]() ,
,![]() 含量为
含量为![]() ,现用方案3提纯10L该粗盐水,求需要加入石灰乳(视为
,现用方案3提纯10L该粗盐水,求需要加入石灰乳(视为![]() )和碳酸钠的物质的量_______。
)和碳酸钠的物质的量_______。
三、溴化铝的性质
7. 已知![]() 可二聚为下图的二聚体:
可二聚为下图的二聚体:
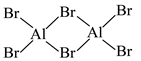
(1)该二聚体中存在的化学键类型为_______。
A. 极性键 B. 非极性键 C. 离子键 D. 金属键
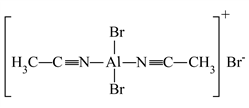
(2)将该二聚体溶于![]() 生成
生成![]() (结构如图所示),已知其配离子为四面体形,中心原子杂化方式为_______,其中配体
(结构如图所示),已知其配离子为四面体形,中心原子杂化方式为_______,其中配体![]() _______,
_______,![]() 该配合物中有
该配合物中有![]() 键_______
键_______![]() 。
。
8. I.铝的三种化合物的沸点如下表所示:
铝的卤化物 |
|
|
|
沸点 | 1500 | 370 | 430 |
(1)解释三种卤化物沸点差异的原因_______。
(2)已知反应![]() 。
。
①![]()
②![]()
③![]()
④![]()
⑤![]()
则![]() _______。
_______。
(3)由图可知,若该反应自发,则该反应的_______。

A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
II.已如![]() 的晶胞如图所示(已知结构为平行六面体,各棱长不相等,
的晶胞如图所示(已知结构为平行六面体,各棱长不相等,![]() 在棱心)
在棱心)
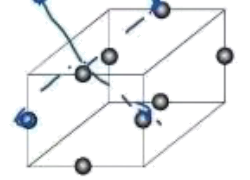
(4)该晶体中,每个![]() ,距离其最近的
,距离其最近的![]() 有_______个。
有_______个。
A. 4 B. 5 C. 8 D. 12
(5)已知![]() ,一个晶胞的体积
,一个晶胞的体积![]() 。求
。求![]() 的晶胞密度_______。
的晶胞密度_______。
(6)![]() 水解可得
水解可得![]() 胶体,请解释用
胶体,请解释用![]() 可净水的原因_______。
可净水的原因_______。
(7)用上述制得的胶体做电泳实验时,有某种胶体粒子向阴极移动,该粒子可能是_______。
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
四、瑞格列奈的制备
9. 瑞格列奈的制备。

(1)瑞格列奈中的含氧官能团除了羧基、醚键,还存在_______。
(2)反应①的反应类型为_______。
A. 还原反应 B. 消去反应 C. 取代反应 D. 氧化反应
(3)反应②的试剂和条件是_______。
(4)D的分子式是![]() ,画出D的结构简式_______。
,画出D的结构简式_______。
(5)化合物D有多种同分异构体,写出满足下列条件的D的同分异构体的结构简式_______。
i.芳香族化合物,可以发生银镜反应;
ii.核磁共振氢谱中显示出3组峰,其峰面积之比为![]() 。
。
(6)G对映异构体分离后才能发生下一步反应
①G中有_______个手性碳
②已知 ,用
,用 和谷氨酸可制备
和谷氨酸可制备 ,该物质可用于分离对映异构体。谷氨酸的结构简式为:_______。检验谷氨酸的试剂是_______。
,该物质可用于分离对映异构体。谷氨酸的结构简式为:_______。检验谷氨酸的试剂是_______。
A. 硝酸 B. 茚三酮 C. ![]() D.
D. ![]()
(7)用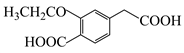 与G可直接制取H。但产率变低,请分析原因_______。
与G可直接制取H。但产率变低,请分析原因_______。
(8)以![]() 和
和![]() 合成
合成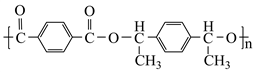 _______。
_______。
五、珊瑚的形成与保护
10. 已知:![]()
①![]()
②![]()
③![]()
(1)以下能判断总反应达到平衡状态的是_______。
A. 钙离子浓度保持不变 B.  保持不变
保持不变
C. ![]() D.
D. ![]()
(2)![]() 增大有利于珊瑚的形成,请解释原因_______。
增大有利于珊瑚的形成,请解释原因_______。
(3)已知![]() 的
的![]() ,
,![]() 为_______。当
为_______。当![]() _______
_______![]() 时,开始产生
时,开始产生![]() 沉淀。
沉淀。
(4)根据如图,写出电极a的电极反应式_______。
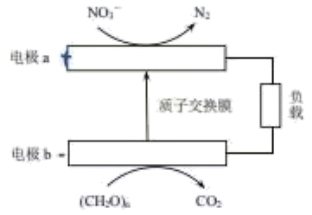
(5)关于上述电化学反应过程,描述正确的是_______。
A. 该装置实现电能转化为化学能
B. 电极b是负极
C. 电子从电极a经过负载到电极b再经过水体回到电极a
D. 每![]() 参与反应时,转移
参与反应时,转移![]() 电子
电子
(6)解释在溶液中氧气的浓度变大后,为何有利于![]() 的除去,但不利于硝酸根的除去。_______。
的除去,但不利于硝酸根的除去。_______。
参考答案
一、氟及其化合物
氟元素及其化合物具有广泛用途。
【1题答案】
【答案】C
【2题答案】
【答案】D
【3题答案】
【答案】 ①. ![]() ②. BC
②. BC
【4题答案】
【答案】 ①. H2F ②. 氢键
【5题答案】
【答案】(1)氟单质与铜制容器表面的铜反应形成一层保护性的氯化铜薄膜,可阻止氟与铜进一步反应 (2)A (3)AB
(4)![]()
二、粗盐水的精制
【6题答案】
【答案】(1)取少量该步骤所得的上清液于试管中,再滴入几滴稀硫酸溶液,若溶液未变浑浊,表明BaCl2已过量 (2)AD (3)B
(4)![]() 、
、![]() (5)C
(5)C
(6)![]() 、
、![]()
(7)提纯粗盐的同时,可变废为宝,将含NH3和CO2的工业废气转化为氮肥,同时减少了废气的排放,有利于保护环境
(8)0.04mol;0.14mol
三、溴化铝的性质
【7题答案】
【答案】(1)A (2) ①. sp3 ②. CH3CN ③. 14
【8题答案】
【答案】(1)AlF3为离子晶体,AlCl3和AlBr3为分子晶体,故AlF3的沸点最高;AlBr3的相对分子质量大于AlCl3,故AlBr3的分子间作用力大于AlCl3,所以AlBr3的沸点高于AlCl3。
(2)![]() (3)A (4)A
(3)A (4)A
(5)3.24g・cm-3
(6)氢氧化铝胶体粒子有很大的比表面积,具有较好的吸附性,能吸附水中的悬浮颗粒并使其沉降,因而常用于水的净化 (7)A
四、瑞格列奈的制备
【9题答案】
【答案】(1)酰胺基 (2)A
(3)稀硫酸、加热或者NaOH溶液、加热/H+
(4) (5)
(5) (6) ①. 1 ②.
(6) ①. 1 ②. 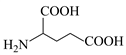 ③. B
③. B
(7)该物质中有2个羧基都会生成酰胺基,所以与G反应会产生副产物,产率变低
(8)
五、珊瑚的形成与保护
【10题答案】
【答案】(1)AB (2)pH越大,即c(H+)越小,促进![]() 的平衡正向移动,即
的平衡正向移动,即![]() 增大,方程式
增大,方程式![]() 平衡正向移动,有利于生成CaCO3;
平衡正向移动,有利于生成CaCO3;
(3) ①. ![]() ②. 4.2×10-3
②. 4.2×10-3
(4)![]() (5)B
(5)B
(6)氧气浓度变大后,O2在正极放电,使得硝酸根的去除率减小,等物质的量的O2得电子的数目大于![]() ,使得转移电子数增大,有机物的去除率增大
,使得转移电子数增大,有机物的去除率增大
